
无论是临床研究还是日常实践,不同患者之间,甚至是同一名患者,对精神科药物的应答(包括疗效及副作用)均可能存在差异。目前,尚无预测具体患者治疗转归的工具,原因在于导致这些差异的原因及其来源均不明确。著名精神药理学专家Sheldon H. Preskorn博士试图通过病例对导致抗抑郁药及抗精神病药应答差异的原因进行阐述,以下为内容要点。

病例一:遗传因素如何影响抗抑郁药应答?
患者男,40岁,罹患重性抑郁症(MMD),使用文拉法辛治疗,滴定至300mg/d。尽管已达足量足疗程治疗,依从性也较为理想,但无治疗获益。基因型检测提示,患者为CYP2D6弱代谢(PM)个体。
讨论
这一病例可用近期发表的一项针对既往4项研究的数据再分析加以解释。这4项针对文拉法辛的研究在设计及方法学上如出一辙,于上世纪90年代中期递交FDA,作为批准该药注册的支持性证据。之所以专门选择这4项研究,是因为这些研究采集了受试者的血样,并测定了文拉法辛及去甲文拉法辛的血药水平;而之所以进行本项再分析,是因为人们后来发现,去甲文拉法辛与文拉法辛血药浓度的比值是确定CYP2D6 强代谢(EMs)与弱代谢(PMs)基因型的途径之一。
结果显示,CYP2D6 EMs个体文拉法辛的净应答/缓解率(文拉法辛应答/缓解率-安慰剂应答/缓解率)为CYP2D6 PMs个体的2.5-3倍(P<0.01)。另外,EMs个体文拉法辛治疗的应答及缓解率显著高于安慰剂,差异具有统计学意义,而PMs个体则并不显著优于安慰剂。
本项再分析并未确定上述发现的潜在原因,目前至少有两种解释:1、CYP2D6 PMs个体对生物胺作用机制的抗抑郁药并不能产生应答;2、文拉法辛需要首先在体内转化为去甲文拉法辛,方可发挥作用。本项研究观察到了现象,但并未给出解释。然而,据作者Preskorn博士所知,这也是迄今为止所确定的、遗传因素对抗抑郁药疗效影响最为显著的个案。
病例二:环境因素如何“模拟”遗传差异?
患者女,45岁,2年前接受雌激素/孕激素受体阳性乳腺癌的外科切除手术,目前正在使用他莫昔芬进行维持治疗,同时使用帕罗西汀40mg/d治疗复发性抑郁障碍。尽管持续使用他莫昔芬,患者还是遭遇了乳腺癌的复发,并最终死于该病。
讨论
以下事实与上述临床个案相关:首先,他莫昔芬必须在体内转化为活性代谢产物endoxifen,方可发挥对抗乳腺癌的疗效,这一过程依赖于CYP2D6所介导的药物氧化代谢过程。事实上,CYP2D6 PMs个体发生他莫昔芬治疗失败的风险更高,包括肿瘤复发及死亡所经历的时间。帕罗西汀可导致个体的CYP2D6表型转化为PM状态,而另一项药物流行病学研究也显示,联用帕罗西汀及他莫昔芬可升高后者治疗失败的风险,患者的生存时间也更短。
对于本例患者而言,其本身属CYP2D6 EMs还是PMs个体并不重要;该患者所服用的帕罗西汀剂量已足以将几乎所有CYP2D6 EMs及中间型代谢(IMs)个体转化为表型上的PMs个体。这一个案提示,预测治疗转归时为何必须考虑多重用药的影响,而一种精神科药物也可能导致非精神科药物治疗的失败。另外,类似患者使用帕罗西汀这样的抗抑郁药的机率也较高,因为这些药物除了治疗抑郁障碍外,也可用于治疗潮热症状。
这一病例发生在我们对他莫昔芬在体内的转化过程有所了解之前,因此并不构成医疗差错。现在,我们已经知道了上述事实,他莫昔芬包装内的说明也进行了相应的修订,而有关药物-药物及基因-药物相互作用的软件包也加入了相关警告。
病例三:遗传、环境及疾病多重因素如何影响药物应答?
患者男,66岁,白人,罹患精神病性抑郁,使用帕罗西汀40mg/d及伊潘立酮24mg/d治疗成功,目前正在使用上述药物进行维持治疗。患者后来罹患支气管炎,其内科医师使用了克拉霉素,250mg bid,为期14天。在抗生素治疗第1周结束时,患者于精神科医师处常规复诊,一般状况良好,只是近期出现了数次间歇性头晕,其中一次接近昏厥。患者共病2型糖尿病,使用二甲双胍控制良好;共病肥胖;4年前接受冠状动脉搭桥术。
讨论
基于我们对伊潘立酮药理学的知识,该患者发生一种致命的心律失常,即尖端扭转型室性心动过速(TdP)的风险升高。事实上,可能正是这一原因导致患者接近晕厥的发作。该患者可行心电图检查,观察QTc间期的情况。
这一病例在很大程度上可以被FDA所命名的“thorough QTc”研究所解释,这些研究旨在评估药物所导致的具有临床意义的QTc间期延长。研究设计包括:(1)受试者被随机分入三种剂量的伊潘立酮组,以及安慰剂组及活性对照组(如喹硫平和齐拉西酮);(2)使用超过一般治疗剂量的伊潘立酮(如24mg/d);(3)首先单独使用伊潘立酮,随后联用CYP2D6抑制剂(如帕罗西汀),再进一步联用CYP3A4抑制剂酮康唑,即患者同时接受伊潘立酮、帕罗西汀及酮康唑治疗。最后,研究者测定了所有受试者的相关基因型,包括CYP2D6及电压门控钾通道KCNQ基因:后者的变异是药物相关长QT间期综合征,包括TdP的素因。
QTc间期延长超过60ms被FDA视为具有临床意义的改变,提示药物所致TdP风险。TQT研究中,共有10名个体出现了此种程度的延长。这些患者与6个变量相关:(1)使用伊潘立酮治疗;(2)使用24mg/d;(3)联用帕罗西汀;(4)联用酮康唑;(5)CYP2D6处于PM状态;(6)具有对QT延长易感的KCNQ基因型。没有一名患者同时满足上述6个条件;事实上,只要具备上述2个或3个条件就足够发展出QTc间期延长。换言之,同一种不良治疗转归可由于多种因素的不同组合而导致,包括状态(state)及特质(trait)变量。
在前两个病例的基础上,该个案进一步提示了预测精神科药物治疗应答的复杂性。如果将伊潘立酮剂量下调,患者可能会安然无恙,但或许也得不到治疗所需的应答。
病例四:药物剂型改变及患者生理状态如何解释严重不良事件?
患者男,18岁,高中生,正在接受一种SSRI、喹硫平300mg/d、一种苯二氮䓬类药物及苯海拉明治疗,时间超过2周。最近7天内,患者出现恶心,饮食减少,体重下降3kg;血压较前下降,目前为102/76mmHg,心率增加至92bpm。需要指出的是,患者是一名长跑运动员,其一般状况下的血压为120/60mmHg,心率为55bpm。出事当晚,患者所服用的喹硫平由缓释片(ER)换为速释片(IR);服药后,患者随即在一张躺椅上以半卧位入睡。次日早晨,其他人发现患者呼之不应,最终诊断为吸入性肺炎。
讨论
本例个案中,遗传因素所扮演的角色并不突出,真正起作用的因素包括:(1)先前既已存在的脱水,导致血压下降及心率的代偿性升高;(2)从ER到IR剂型的转换导致血药浓度达峰所需时间缩短,且峰值达到2.5-3倍之高,进而导致更为严重的α1受体阻断效应;(3)半卧位导致血流聚集于下肢;(4)联用苯二氮䓬及苯海拉明;(5)高剂量喹硫平导致更强的D2受体阻断效应,进而造成疑似呕吐反射损害。
这一个案的关键点在于,个体内在环境的改变(脱水)如何与服药剂型的改变联合,对不良转归的发生导致了深远的影响。
结论
本文的主题在于,“个体化治疗”的概念并不仅仅建立在遗传差异的基础上;事实上,患者所处的生理状态,包括年龄、共病、联用药物等均须加以考虑。这一主题并不算新颖:早在100多年前,Claude Bernard即警告医师,须意识到每位患者都是独一无二的,而他们的独特性也可能随着时间的流逝而变化。
临床医师应使用自己的决断、知识及经验,综合考虑所有导致个体间及同一个体间应答差异的来源。通过监测患者,医师可进一步调整治疗,即便是在差异化原因尚未得到充分理解的情况下。
文献索引:Preskorn SH et al./Prediction of individual response to antidepressants and antipsychotics: an integrated concept. Dialogues Clin Neurosci. 2014 Dec;16(4):545-54.
医脉通编译,转载请注明出处。
一般而言,若抑郁患者对至少两种不同类型抗抑郁药足量足疗程治疗应答欠佳,即被视为难治性抑郁。尽管在临床试验中,抗抑郁药的疗效总体相仿,但这些药物不同的作用机制(MOA)决定了其针对不同症状患者的疗效的好坏。为帮助难治性抑郁患者获得更好的转归,不同种类抗抑郁药的MOA也应加以考虑。
MOA的重要意义
抑郁是一种异质性很强的疾病,不同亚型抑郁的病因学可能存在差异,所影响的脑区也有所不同。与此同时,抗抑郁药也可通过不同的途径影响大脑。了解不同抗抑郁药所影响的通路,有助于提高临床医师治疗难治性抑郁的能力。
所有抗抑郁药均存在安慰剂效应,临床实验中其比重约为30-40%。除此之外,其MOA决定了具体每种抗抑郁药可能对哪些特定患者群体疗效更佳。抗抑郁药的副作用同样与MOA有关,而副作用也同样可能为我们所用。例如,镇静副作用或有助于帮助那些睡眠困难的患者。
单胺通路是一个好的开始。很多传统抗抑郁药通过增强5-HT及NE能传递,与抑郁病因学通路发生相互作用,进而发挥疗效。具体而言:
★ 主要调节5-HT能的药物:有助于减弱过度的负性情感反应;
★ 主要调节NE能的药物:有助于改善积极情感、精力及注意集中;
★ 主要调节DA能的药物:目前尚无此类抗抑郁药,但DA对于驱力、犒赏及动机关系具有重要影响。
目前,大部分抗抑郁药主要作用于5-HT及NE能,而对DA能传递仅有间接作用,这或许可以解释为什么动机及快感受损常成为抑郁残留症状。可同时抑制三种单胺的抗抑郁药,包括DA,或许可以提供较传统抗抑郁药更为理想的抗抑郁功效,尤其是非典型抑郁及带有忧郁特质的抑郁患者。此类药物目前正在研发之中。
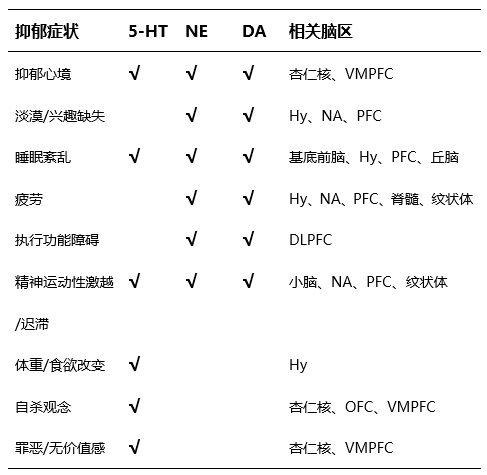
VMPFC:腹内侧前额叶皮质 Hy:下丘脑 NA:伏隔核 PFC:前额叶皮质 DLPFC:背外侧前额叶皮质
单胺假说
经典的单胺假说指出:当单胺活性正常时,个体无抑郁表现;但如果5-HT及NE水平下降,抑郁症状即表现出来。因此,抗抑郁药可通过升高突触间隙单胺浓度而改善抑郁症状。
而目前的单胺假说指出,脑内DA、NE及5-HT受体改变可导致抑郁;特别指出,受体浓度过高可导致抑郁。
经典单胺假说诞生于人们意识到DA、谷氨酸及特定神经肽在抑郁中所扮演的角色之前。由于最初的抗抑郁药可提高或修复NE及5-HT水平,上世纪60年代及70年代早期,人们认为抑郁的病因已被发现,因而乐观情绪弥漫。然而目前,人们发现抑郁的机制远比预想复杂,单胺假说也并不能很好地解释抗抑郁药的起效。不过,三种关键单胺通路仍值得研究,因为其与MDD症状存在潜在联系。
多巴胺(DA)
DA与警戒性、警觉、驱力及动机相关。理论上讲,那些主要表现为动机及兴趣下降的患者可能存在多巴胺能缺陷。伏隔核活动下降可能导致个体出现淡漠,而这一生理状况可能是持续的、难以解决的应激的产物;换言之,如果个体持续面临看上去难以解决的重大问题,而不对其加以解决的后果是严重的,那么个体即没有寻找乐趣或犒赏活动的即刻需要。
一些抗抑郁药对DA能的作用强于其他药物。在传统抗抑郁药中,单胺氧化酶抑制剂(MAOIs)的多巴胺能效应最强,因为此类药物可减少突触DA的降解。新型抗抑郁药中,安非他酮的多巴胺能效应最强,但PET成像却显示,该药的多巴胺效应相对比较温和。SNRIs类药物文拉法辛在很高的剂量下具有轻度的DA能效应,而SSRIs类药物舍曲林在高剂量下也可抑制DA能再摄取。若希望强调DA能效应,则需要联用神经兴奋剂或第二代抗精神病药,例如低剂量的阿立哌唑。
去甲肾上腺素(NE)
NE与精力下降及注意力集中问题相关。NE减少,尤其是前额叶皮质处的NE减少,可能导致警觉性、注意力集中、决策及信息处理方面的问题。上述症状可见于ADHD及抑郁患者中。
多种药物可以升高NE水平。三环类抗抑郁药(TCAs)主要作用于NE能;对于大部分TCAs而言,其对NE再摄取抑制的选择性高于5-HT。新型抗抑郁药中,安非他酮及SNRIs具有NE能效应。
5-羟色胺(5-HT)
存在5-HT功能异常的患者可能表现出悲哀、伤感、罪恶感或自杀倾向。5-HT能通路与NE能位于同一位置。存在强烈负性情感的患者可能存在5-HT能低下,进而无法发挥对负性情感的抑制作用。
很多药物可增强5-HT能活性,最常使用的一类药物为SSRIs。
病例1 P先生,69岁,丧偶,因失眠、坐立不安、易激惹、体重下降、注意力难以集中及便秘于初级保健医生处就诊。他一方面否认存在自杀观念,而另一方面却又在询问是否还值得活下去,因为他在做生意时犯了一个错误,导致其损失了10万美元。他的子女确信这一事件导致了其父亲的心境改变,尽管他其他的生意进展顺利。P先生目前处于对立、消极和愤怒的状态。 P先生无精神疾病史,也未表现出显著的躁狂、焦虑障碍、进食障碍或物质使用障碍。他的状况满足DSM-5重性抑郁诊断标准,但对于一种常用SSRI及一种常用SNRI足量足疗程治疗无应答。在转诊至精神科医师处、去甲文拉法辛滴定至200mg/d后,P先生的病情仍无显著改善,医师随即加用了米氮平,并滴定至45mg/d。 复诊时,P先生表现显易激惹及紧绷,持续诉说其过往的经济失败、需要自己承担的药费及便秘问题。精神科医师怀疑其可能掺杂有妄想信念,随即停用米氮平,加用了低剂量的阿立哌唑。 阿立哌唑5mg/d及10mg/d时对P先生的帮助微乎其微;然而,一加量至15mg/d,P先生即显得不再那么紧张和焦虑,睡眠也得到了改善。加量至20mg/d时,他承认自己“在经济生活方面并没有那么失败”,“单笔生意损失并不代表着彻头彻尾的失败”。他认识到自己有足够多的钱,完全可以安然退休,无后顾之忧。他不再抱怨自己的消化道及药费问题。数周后,P先生的症状消失,此时用药方案为去甲文拉法辛200mg/d+阿立哌唑20mg/d。 在阿立哌唑加量至治疗精神病的剂量之前,P先生的抑郁对治疗始终无应答。从临床角度而言,他确实存在一些难以被事实所驱散的固着信念,其最终诊断为MDD重度发作,伴精神病性特质。P先生最初看起来是一个难治性抑郁病例,但对阿立哌唑增效治疗应答相当理想,而阿立哌唑是针对其精神病性妄想而使用的。如果更早地将患者认知层面上的问题定性为精神病性症状,P先生的症状或许可以得到更快的缓解。 治疗过程中,两种抗抑郁药可通过不同机制升高NE及HT水平,但对P先生而言并不足够:他所罹患的可能是一种特殊的情感障碍形式,对抗抑郁药治疗较少产生应答。事实上,对于P先生而言,阻断D2受体以消除抑郁中的精神病性组分,而非激活DA能,是获得较为完全的抗抑郁效应的必由之路。 目前,尚无第二代抗精神病药被专门批准治疗MDD伴精神病性特质。然而,从上世纪80年代开始,我们已经知道,此种MDD对包含有抗精神病药的治疗方案应答更佳,优于抗抑郁药单药治疗。本例患者对SRIs单药治疗应答不佳,提示5-HT能异常并非其抑郁的主因,也必然不是其精神病的病因。因此,其精神病在理论上与其边缘系统DA活动增强相关。 |
文献索引:Thase ME et al. Choosing medications for treatment-resistant depression based on mechanism of action. J Clin Psychiatry. 2015 Jun;76(6):720-7. doi: 10.4088/JCP.14052ah2c.
医脉通编译,转载请注明出处。
传统抗抑郁药
三环类抗抑郁药(TCAs)
★ 双通道机制,同时抑制NE及5-HT再摄取,并对其他多种递质系统发挥效应;
★ 由于副作用及潜在过量死亡风险,已不作为临床首选;
★ 主要用于难治性抑郁患者。
TCAs的发现属于机缘巧合:上世纪50年代,人们致力于研发更安全的抗精神病药,结果偶然发现了TCAs。目前,被FDA批准上市的TCAs包括丙咪嗪、阿米替林、地昔帕明、多塞平、去甲替林、氯米帕明等。由于结构类似,阿莫沙平与马普替林有时也被划归TCAs中。
TCAs非选择性地抑制NE再摄取,并不同程度地抑制5-HT再摄取。此外,此类药物对组胺、胆碱能等其他一系列受体均有一定效应。尽管TCAs曾被视为抑郁一线治疗选择,但目前一般仅应用于难治性患者;由于其副作用及潜在的过量死亡风险,此类药物在治疗方案中所处的位置比较靠后。TCAs的常见副作用包括口干、视物模糊、便秘、心动过缓、镇静、体重增加及低血压。对于50岁以上的患者,用药前应行心电图检查,如果患者出现头晕,还应针对直立性低血压展开监测。
TCAs主要针对NE能,但氯米帕明是个例外:该药具有较强的5-HT能效应,以及NE能效应,使得该药可以为严重抑郁或强迫障碍(OCD)患者带来收益。尽管并非高度选择性的药物,但去甲替林和地昔帕明可被视为久经考验的NE再摄取抑制剂,配合适当监测,可以与SSRIs联用,有时也可与MAOIs联用。
单胺氧化酶抑制剂(MAOIs)
★ 可抑制5-HT、NE及DA等多种神经递质的代谢,进而升高其水平;
★ 患者须严格遵循饮食及联合用药禁忌;
★ 其他类型抗抑郁药应答不佳的患者使用MAOIs可能非常有效,尤其是非典型抑郁。
此类药物来源于一个发现:抗结核药物可改善抑郁症状。若TCAs难以奏效,MAOIs随即跟上,因为此类药物可升高5-HT、NE及DA水平,这一多重作用机制使得MAOIs成为那些对TCAs的NE能效应无应答的患者的又一治疗选择。
非选择性MAOIs(同时抑制MAO-A及MAO-B)包括苯乙肼、异卡波肼及反苯环丙胺。司来吉兰有时被划归为选择性MAOIs,因为该药在低剂量时仅抑制MAO-B;然而,被批准用于治疗帕金森病的司来吉兰在如此低的剂量下可能并不具有抗抑郁功效。此类药物可抑制MAO-A代谢5-HT、NE、DA及酪胺,抑制MAO-B代谢苯乙胺、DA及酪胺,这种抑制作用可能造成肠道内的酪胺无法被降解,进而导致特殊的作用。因此,使用MAOIs的患者须遵循低酪胺饮食,避免使用成熟干酪、大豆制品、啤酒及某些特定的酒类。然而,使用司来吉兰透皮贴剂无须规避上述饮食禁忌。
鉴于可能导致5-HT综合征,具有较强5-HT能效应的药物禁止与MAOIs联用。5-HT综合征由5-HT水平过高引起,主要症状包括腹痛、腹泻、出汗、无精打采、震颤、精神状态改变及心血管休克。MAOIs的镇静效果总体弱于TCAs,常见副作用包括低血压、体重增加、性功能障碍、头痛及失眠。
尽管存在饮食及药物联用禁忌,MAOIs对于那些对其他类型抗抑郁药应答不佳的患者非常有效。治疗优先级方面,MAOIs通常在TCAs之后;然而,对于非典型抑郁,MAOIs可在TCAs之前使用:前者针对此类患者的疗效优于后者。非典型抑郁的主要表现为心境反应性、灌铅样麻痹、对拒绝的过度敏感,以及体重、食欲及睡眠增加。
新型抗抑郁药
NE及DA再摄取抑制剂(NDRIs)
★ 几无5-HT能效应,主要抑制NE及DA再摄取,但效应较弱;
★ 无性功能副作用。
唯一一种获FDA批准治疗MDD的NDRI为安非他酮,该药于1985年被首次引入市场,为最早问世的新型抗抑郁药。安非他酮速释制剂每天需服用3次,且惊厥风险较高,因而自动撤市,但随后以缓释剂的新剂型回归市场,最大剂量为450mg/d,这也降低了惊厥风险。安非他酮几无5-HT能效应,主要抑制NE及DA再摄取,但上述效应均较弱,其代谢产物被认为与抗抑郁疗效相关。
安非他酮的副作用包括头痛、头晕、恶心、口干、失眠及瘙痒;该药无性方面的副作用,很大程度上是因为该药不抑制5-HT再摄取,对于那些使用SSRIs出现显著性功能障碍的患者而言,该药可作为替代治疗的选择。
选择性5-HT再摄取抑制剂(SSRIs)
★ 一线抗抑郁治疗中的一线药物;
★ 选择性抑制5-HT再摄取,疗效确切,耐受性良好;
★ 主要用于病情相对较轻的患者,治疗严重抑郁的疗效不及TCAs。
作为第一种SSRIs,氟西汀于上世纪八十年代末首次引入市场。进入21世纪,此类药物已成为使用最为广泛的一类抗抑郁药。在大部分诊疗流程中,SSRIs均为一线中的一线药物。此类药物包括西酞普兰、艾司西酞普兰、氟西汀、帕罗西汀、舍曲林及氟伏沙明,但氟伏沙明并未被FDA批准治疗MDD。顾名思义,SSRIs选择性抑制5-HT再摄取。除了已经得到充分验证的抗抑郁疗效外,此类药物已成为多种焦虑障碍的一线治疗药物,这一点对于抑郁共病或继发焦虑障碍患者尤为受用。
SSRIs相关副作用包括体重增加、口干、恶心、头痛、睡眠问题及性功能障碍。尽管存在上述副作用,但SSRIs过量时的安全性优于TCAs,相比于TCAs及MAOIs使用更为容易及安全。由于作用机制较为简单,SSRIs的耐受性相当好;在大部分患者中,SSRIs起始剂量即为有效剂量。这一点与TCAs及MAOIs形成鲜明对比:后者必须逐渐滴定至治疗剂量。
与传统抗抑郁药不同,SSRIs常用于症状相对较轻的抑郁患者。对于严重抑郁患者,TCAs类抗抑郁药氯米帕明的效果优于SSRIs。
5-HT/NE再摄取抑制剂(SNRIs)
★ 与TCAs类似,属于双通道药物,但选择性更高,因而耐受性更佳;
★ 针对严重抑郁患者,文拉法辛的疗效弱于某些TCAs,但可能优于SSRIs;
★ 具体SNRIs的疗效是否优于SSRIs,目前仍存在争议;
获FDA批准治疗抑郁的SNRIs包括文拉法辛、去甲文拉法辛、度洛西汀及左旋米那普仑。与TCAs类似,SNRIs属于双通道药物,但选择性更高,进而在保留治疗效应的同时减少了不良反应。度洛西汀和文拉法辛的NE再摄取抑制效应可能弱于某些TCAs,进而导致前两种药物在治疗严重抑郁时不如TCAs有效;然而,针对此类抑郁患者,文拉法辛的疗效仍优于SSRIs。SNRIs的副作用与SSRIs类似。
尽管SNRIs类研发的发生点在于在SSRIs的基础上增加一种MOA以增强抗抑郁疗效,但至于这一目标究竟是否真的实现了,目前人们仍争论不休。其中一部分原因在于,我们难以确定新增加的NE能效应何时开始起效。证据提示,SNRIs平均而言略优于SSRIs,但证据效力在不同SNRIs中并不等同。如前所示,不同的抑郁症状可能对不同的抗抑郁药应答更好(病例2);例如,SNRIs可能更适用于存在显著疼痛症状的患者,而度洛西汀已被批准治疗多种疼痛相关的适应征。
多机制抗抑郁药
此类抗抑郁药可调控不同受体,包括米氮平、曲唑酮、萘法唑酮、维拉唑酮及沃替西汀。除米氮平之外,其他药物均在5-HT再摄取抑制的基础上叠加了其他作用机制。
米氮平有时被称为“NE/特异性5-HT能抗抑郁剂”(NaSSA)。该药并非再摄取抑制剂,其5-HT及NE能效应来自继发机制。作为一种强效抗组胺药,米氮平是新型抗抑郁药中镇静效果最强的,可导致体重增加及日间嗜睡。
与米氮平不同,曲唑酮及结构与之类似的萘法唑酮均为较弱的5-HT能再摄取抑制剂,可阻断5-HT2A及2C受体,被归类为5-HT拮抗/再摄取抑制剂(SARIs)。曲唑酮及萘法唑酮均具有较强的镇静效应,其他常见不良反应包括恶心、头晕、便秘及视物模糊。目前,低剂量(25-100mg)曲唑酮常被超适应征应用于镇静,但在剂量较高(150-600mg/d)时,该药是一种有效的抗抑郁剂。
由于性副作用风险低及良好的睡眠效应,萘法唑酮一度被广泛使用。然而,该药在今天已极少使用,原因在于其肝毒性。
除5-HT再摄取抑制外,维拉唑酮还可部分激动5-HT1A受体。该药的副作用包括轻度腹泻及恶心;相比于其他抗抑郁药,该药体重增加及性功能障碍发生的风险较低。
沃替西汀是一种5-HT再摄取抑制剂,同时对于5-HT1A/1B、5-HT3、5-HT7受体具有复杂的效应,进而可能有利于存在认知症状的抑郁患者。总体而言,上述药物为不能耐受SSRIs及SNRIs的患者提供了有用的替代治疗选择。
病例2 M女士,36岁,已婚育有2子女,平面艺术家及网站设计师,由其心理治疗师转诊至精神科医生处。前者建议重新评估其心境障碍及治疗:治疗师认为M女士罹患复发性抑郁,还可能存在环形人格。 M女士的自杀、抑郁及酒药滥用家族史阳性。其首次抑郁发作发生于16岁时,此后又至少出现过4次抑郁发作,其中包括2次产后抑郁。较早的发作对心理治疗及氟西汀可产生应答,但每次均出现复发,其中一次发生于她正在服用氟西汀40mg/d时。需要指出的是,她当时还被诊断为甲减,而T4治疗在一定程度上改善了其生活治疗,并阻止了体重的增加。氟西汀基础上联用安非他酮150mg/d bid之后,M女士的病情似乎有所改善,但随后却出现了惊恐发作、严重失眠及烦躁,最终导致联合治疗的中止。她继续坚持心理治疗,并在此后的若干年内保持了较好的状态,但在秋冬季,她仍能体验到轻度的抑郁。 针对M女士的最近一次抑郁发作,治疗药物为文拉法辛缓释剂型,剂量为75mg/d;治疗仅2周,M女士即自感“显著改善”。然而,M女士的爱人打电话报告称,M女士表现得易激惹,睡眠少;在随后的复诊中,医生停用了文拉法辛。 2个月后,M女士出现了精力及兴趣下降的表现。通过进一步询问,精神科医师发现,文拉法辛实际上导致了一次轻躁狂发作。 M女士最初表现为复发性抑郁,且在服用足量抗抑郁药的情况下复发。然而,M女士也的确表现出一些双相抑郁的特质:首次重性抑郁发作年龄小、环形气质、超过3次重性抑郁发作、抗抑郁药所致轻躁发作、产后抑郁及症状的季节性。精神疾病史及当前的症状显示,M女士的抑郁掺杂了轻躁特质。其最终的诊断为:双相障碍 II 型。 M女士换用了一种心境稳定剂,联合心理治疗;对于双相障碍而言,上述治疗手段优于抗抑郁药。一些双相抑郁患者对抗抑郁药应答相当理想,但另一些人则可能发展为快速循环或在治疗过程中出现心境转相。与SSRIs及安非他酮相比,双通道的SNRIs及TCAs似乎更容易导致上述不愉快的结果。治疗抑郁时,临床医师必须始终评估躁狂及轻躁狂风险,以确认排除了双相障碍的可能;若抗抑郁药为治疗所必需,那么医生对于心境稳定剂预防治疗也应有所准备。 |
结语
很多抑郁患者存在难治性症状。通过考虑与患者特异性症状可能相关的单胺能通路功能异常,临床医师可以有针对性地选择5-HT、NE及DA的药物。不同的抗抑郁药种类与3种单胺通路的特异性改变相关,改变这些通路可能带来治疗获益,以及相应副作用。
选择性较差的抗抑郁药可能带来耐受性问题,如TCAs及MAOIs,但上述药物对于那些对SSRIs及SNRIs应答不佳的一组患者有效。其他具有选择性机制的药物可能对包括失眠、认知问题及性功能障碍在内的问题具有独到的优势。临床医师有望通过考虑抗抑郁药的MOA解决旷日持久的战斗。
文献索引:Thase ME et al. Choosing medications for treatment-resistant depression based on mechanism of action. J Clin Psychiatry. 2015 Jun;76(6):720-7. doi: 10.4088/JCP.14052ah2c.
医脉通编译,转载请注明出处。
废躯 发表于 15-12-12 17:20
一般而言,若抑郁患者对至少两种不同类型抗抑郁药足量足疗程治疗应答欠佳,即被视为难治性抑郁。尽管在临床 ...
| 欢迎光临 阳光工程心理网 (http://sunofus.org/bbs/) | Powered by Discuz! X3.2 |